특허 풀린 지 7개월 만에 ‘삭센다’ 복제약 첫 승인, FDA “GLP-1 공급 부족 해소 기대”
입력
수정
리라글루티드· 세마글루타이드 등 특허 만료 FDA, 빅토자·삭센다 제네릭 품목으로 허가 英 히크마 파마슈티컬스에서 복제해 제네릭 승인
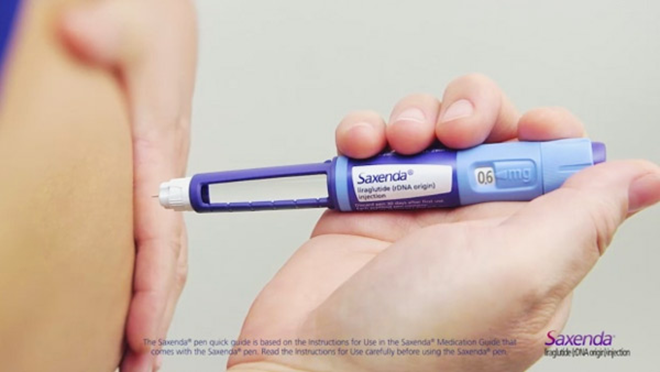
1세대 비만 치료제의 복제약(제네릭)이 미국에서 처음으로 승인됐다. 제네릭은 특허가 만료된 오리지널 의약품의 공개된 기술을 이용해 만든 것으로, 업계는 이번 승인이 리라글루타이드 기반 약물의 공급 부족 문제를 완화하고 환자들에게 더 저렴한 치료 옵션을 제공할 수 있는 계기가 될 것이라 기대하고 있다.
리라글루타이드 제네릭 허가
27일 의약품업계에 따르면 미국 식품의약국(FDA)은 23일(현지시각) 10세 이상 제2형 당뇨병 환자 치료제인 빅토자(성분명 리라글루타이드)의 제네릭 품목을 허가했다. 같은 성분으로 뒤에 나온 것이 비만약 삭센다여서 곧 FDA가 제네릭을 비만 치료제로도 승인할 것으로 기대된다. 영국 히크마 파마슈티컬스가 개발한 빅토자 제네릭은 올 연말까지 미국 전역에 출시할 예정이다.
제네릭 의약품은 원조 의약품과 동일한 성분, 제형, 용법 등으로 만들어진 의약품이다. 원조 의약품의 특허가 만료되면 여러 제약사가 공개된 기술로 제네릭 의약품을 만들 수 있다.
이번 승인은 빅토자의 물질 특허가 만료된 지 약 7개월 만에 이뤄졌다. FDA가 글루카곤 유사 펩타이드(GLP)-1 계열의 제네릭 의약품을 승인한 것은 영국 아스트라제네카의 당뇨병 치료제 바이에타(엑세나타이드)를 복제한 미국 암닐의 제네릭 의약품을 승인한 데 이어 두 번째다.
인체의 GLP-1 호르몬은 혈당을 조절하는 인슐린의 분비를 촉진한다. 동시에 위에서 음식물을 소화하는 속도를 늦춰 포만감을 느끼고 식욕을 억제해 체중을 감량하는 효과를 낸다. GLP-1을 모방한 리라글루타이드는 2010년 당뇨병 치료제인 빅토자에 이어, 2014년 비만 치료제 삭센다로 출시됐다. 덴마크 노보노디스크 역시 GLP-1 유사체인 세마글루타이드로 각각 2017년과 2021년 당뇨약 오젬픽과 비만약 위고비를 출시했다.
다만 1세대 GLP-1 계열 약품은 최신 약품보다 뒤떨어진다. 오젬픽·위고비는 주 1회 주사하는 반면 먼저 나온 빅토자·삭센다는 1일 1회 주사한다. 효과 역시 리라글루타이드가 세마글루타이드보다 약하다고 평가된다. 그러나 가격은 미국에서 최소 월 500달러(약 73만원)로, 월 1,000달러(약 145만원)를 훌쩍 넘는 오젬픽·위고비의 절반 수준이다. 이런 이유로 오젬픽·위고비 대신 빅토자·삭센다를 사용하는 환자가 많았다.
특허 만료 앞두고 복제약 개발 가속
이처럼 리라글루타이드는 수요가 크다 보니 특허 만료 전인 지난해 7월 FDA 공급 부족 약물 목록(shortage list)에까지 올랐다. 이 목록에 오른 약물에 대해서는 FDA의 허가를 받은 조제전문약국(compounding pharmacies) 또는 중소 제약사가 한시적으로 제네릭을 만들어 판매할 수 있다. 오젬픽·위고비의 성분인 세마글루타이드도 함께 올랐다.
FDA는 이러한 공급 부족 약물에 대한 제네릭 의약품의 승인을 우선적으로 검토하고 있다. 공급 상황을 개선할 수 있는 데다, 가격이 낮아져 환자들의 약물 접근성이 훨씬 높아지기 때문이다. FDA는 이번에 공식적인 빅토자 제네릭 승인으로 공급 부족 사태가 안정될 것으로 기대하고 있다.
일룬 머피(Iilun Murphy) FDA 약물평가연구센터의 제네릭 의약품 국장은 “환자 접근성을 개선하기 위해 공급 부족 목록에 오른 의약품에 대한 제네릭 의약품 신청을 우선 평가하고 있다”며 “이번 리라글루타이드의 제네릭 승인은 안전하고 효과적이며, 고품질의 제네릭 의약품에 대한 환자의 접근성을 높일 것”이라고 말했다.
격화되는 비만 치료제 경쟁
현재 국내에서는 펩진과 한독이 삭센다 제네릭을 준비 중이다. 펩진은 바이오플러스와 삭센다, 위고비 제네릭을 공동제품화하기로 했으며, 한독은 인도 바이오기업 바이오콘과 계약을 맺고 제네릭을 국내에 들여오기로 했다. 바이오콘은 지난 3월 삭센다 제네릭을 영국에서 허가받았다. 아울러 바이오콘은 미국과 유럽에도 리라글루타이드에 대한 허가 신청서를 제출한 상태다. 한독은 국내 유통과 독점 판매를 맡는다.
한미약품은 자체 파이프라인을 가동해 비만 치료제를 개발 중이다. 한미약품은 차세대 비만치료 삼중작용제(코드명 HM15275)에 대한 주요 비임상 연구결과를 세계 당뇨학회에서 발표했다. 한미의 차세대 지속형 플랫폼 기술 '아실레이션'이 적용된 HM15275는 GLP-1와 위 억제 펩타이드(GIP), 글루카곤(GCG) 등 세 가지 수용체 각각의 작용을 최적화해 비만 치료에 특화돼 있다. 한미약품은 지난 5월 FDA에서 HM15275 임상 1상 시험계획(IND)을 승인 받았고, 6월 중순부터 HM15275 임상 시험에 참여하는 환자 등록을 시작해 첫 투약을 완료했다.
다만 전문가들은 본격적인 가격 인하에는 시간이 걸릴 것으로 보고 있다. 애런 케셀하임(Aaron Kesselheim) 하버드 의대 교수는 25일(현지 시각) 미국 CNN에 “보통 4개 이상의 제네릭 의약품이 시장에 출시돼야 가격이 50~60% 이상 감소하는 효과를 기대할 수 있다”고 설명했다.

















